Les facteurs de nécrose tumorale sont des cytokines pro-inflammatoires. Cela signifie qu'il s'agit de protéines impliquées dans l'inflammation. Deux types de ces cytokines ont été reconnus: le TNF-alpha et le TNF-bêta. Les noms de ces protéines sont des abréviations de facteur de nécrose tumorale, qui signifie facteur de nécrose tumorale. Comment fonctionnent les facteurs de nécrose tumorale? Comment les inhibiteurs du TNF-alpha sont-ils utilisés pour traiter la maladie?
Table des matières
- Qu'est-ce que l'apoptose?
- Comment fonctionnent les facteurs de nécrose tumorale?
- Comment le TNF-alpha affecte-t-il les changements néoplasiques?
- D'où vient le double mécanisme d'action du TNF-alpha?
- Quels symptômes une augmentation des taux de TNF dans le corps provoque-t-elle?
- TNF-alpha en tant que médicament
- Inhibiteurs du TNF-alpha en tant que médicaments
- Inhibiteurs du TNF dans le traitement de la polyarthrite rhumatoïde
- Inhibiteurs du TNF dans le traitement du cancer
- Inhibiteurs naturels du TNF
Les facteurs de nécrose tumorale activent le processus de mort cellulaire suicide planifiée, c'est-à-dire l'apoptose. C'est un mécanisme qui protège le corps contre la multiplication excessive de cellules génétiquement mutées. Lorsque le processus d'apoptose échoue, une carcinogenèse se produit. Les capacités pro-apoptotiques du TNF-alpha ont trouvé une application clinique dans la thérapie anticancéreuse.
L'utilisation de ce médicament, malheureusement, est associée à des effets secondaires graves. Le TNF-alpha n'est que rarement administré localement dans la zone tumorale.
D'autre part, les inhibiteurs du TNF ont un potentiel thérapeutique beaucoup plus large, qui en raison de leurs effets immunosuppresseurs et immunomodulateurs sont couramment utilisés dans le traitement des maladies auto-immunes.
Qu'est-ce que l'apoptose?
L'apoptose joue un rôle important dans le maintien de l'équilibre des processus de création et de mort de cellules dans le corps humain. Le phénomène pathologique résultant de l'inhibition de la mort cellulaire planifiée est la formation de néoplasmes. L'un des mécanismes induisant l'apoptose est l'activation de récepteurs situés dans la membrane cellulaire. Ces structures membranaires sont appelées domaines de mort. Leur activation se produit, entre autres, après la fixation d'une molécule de signalisation appropriée, par exemple le TNF-alpha.
Lorsque l'apoptose est initiée en raison de la stimulation des récepteurs par la substance activatrice, la phase exécutive suit très rapidement. Des enzymes appropriées décomposent les éléments constitutifs des protéines dans la cellule. L'ADN dans le noyau est condensé puis coupé en morceaux. Finalement, la cellule entière se fragmente en corps apopototiques qui sont engloutis par les cellules nourricières immunitaires. Le TNF-alpha sécrété a la capacité d'attirer les neutrophiles et de stimuler la phagocytose. Ceci est important pour éliminer les cellules apoptotiques restantes de la cellule.
En raison du processus d'apoptose, les enzymes cellulaires ne pénètrent pas et les tissus sains ne sont pas endommagés lors de la destruction de la cellule mutée.
Comment fonctionnent les facteurs de nécrose tumorale?
Les facteurs de nécrose tumorale sont produits par les cellules du système immunitaire, principalement les monocytes et les macrophages. La libération de TNF est stimulée par des stimuli tels que:
- endotoxines
- cellules cancéreuses
- toxines bactériennes
- parasites
- virus
- certains médicaments
Le rôle principal du TNF est de réguler l'activité des cellules immunitaires. TNF, qui est une substance endogène, c'est-à-dire pro-inflammatoire, produite par l'organisme. Il a la capacité d'induire de la fièvre, de l'inflammation et d'inhiber le processus de formation du cancer. Il est également impliqué dans le blocage de la réplication virale et dans la production d'une réponse immunitaire sous forme de septicémie.
La recherche montre que la dérégulation de la production de TNF est impliquée dans le développement de nombreuses maladies. Cela comprend la maladie d'Alzheimer, le cancer, la dépression majeure, le psoriasis et les maladies inflammatoires de l'intestin (MICI).
Comment le TNF-alpha affecte-t-il les changements néoplasiques?
Les facteurs de nécrose tumorale sont deux fois opposés à la carcinogenèse. Cela signifie qu'en fonction de la dose, ils peuvent avoir des propriétés anticancéreuses ou stimuler la formation de métastases.
De faibles niveaux de TNF stimulent la croissance de la masse tumorale. Sous son influence, l'apoptose des cellules mutantes est inhibée, tandis que les cellules saines entourant la lésion néoplasique sont affectées. Dans le même temps, les cellules malades adhèrent davantage à l'endothélium vasculaire. Cela conduit à leur voyage à travers les vaisseaux, ce qui entraîne la propagation de changements néoplasiques dans tout le corps. Les niveaux de TNF-alpha augmentent à mesure que certains cancers se développent. Le niveau élevé de cette substance dans le sang montre négativement l'intensification des processus pathologiques. Par conséquent, la détermination de la concentration de TNF-alpha est utilisée dans le diagnostic.
Des concentrations élevées de TNF-alpha induisent une nécrose hémorragique des tumeurs solides. Cette substance endommage l'endothélium des vaisseaux sanguins de la tumeur. Il inhibe également la croissance, la multiplication et la fonction des cellules, malades et saines. Ce fait, entre autres, entraîne la forte toxicité du TNF-alpha utilisé comme médicament anticancéreux.
D'où vient le double mécanisme d'action du TNF-alpha?
Ces deux effets opposés provoqués par le facteur de nécrose tumorale résultent de la réponse dose-dépendante provoquée par la stimulation des récepteurs de la mort par cette substance. Après leur activation, il existe deux voies de développement possibles dans la cellule. L'un d'eux est l'activation de processus visant à défendre la cellule contre la mort. Cela conduit à la synthèse d'une grande variété de protéines impliquées dans la survie et la multiplication des cellules.
La deuxième réaction possible est d'initier la voie apoptotique. Grâce à lui, la multiplication et la différenciation des cellules cancéreuses sont arrêtées. Cependant, la mort cellulaire induite par le TNF joue un rôle mineur par rapport à son rôle prépondérant dans l'inflammation. Le facteur de nécrose tumorale active les cellules du système immunitaire. Il augmente la capacité d'absorption des neutrophiles et stimule la multiplication et la spécialisation des lymphocytes T et B. Ainsi, il aide à éliminer activement les changements néoplasiques.
Quels symptômes une augmentation des taux de TNF dans le corps provoque-t-elle?
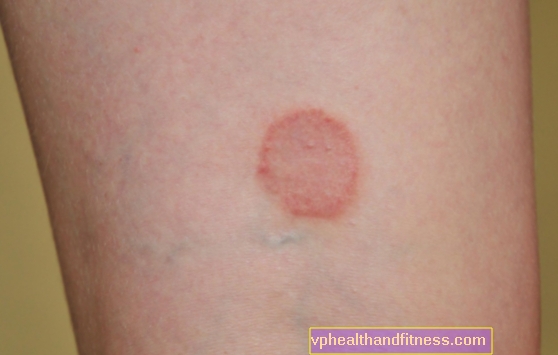
Une augmentation locale de la concentration de TNF provoque les principaux symptômes de l'inflammation:
- température plus élevée
- œdème
- rougissant
- douleur
- perte de fonction d'organe
Des taux systémiques élevés de TNF produisent des symptômes similaires à un choc hypotenseur. Il s'agit d'une condition dans laquelle il y a une défaillance de plusieurs organes et une perte de conscience en raison de la réponse aiguë du corps à cette substance. Par conséquent, le TNF-alpha en tant que médicament anticancéreux n'est administré que localement dans la tumeur.
Une exposition prolongée à de faibles niveaux de TNF se produit pendant le développement du cancer. Une telle présence à long terme d'un facteur de nécrose tumorale élevé provoque un syndrome de dépérissement.
Des niveaux accrus de TNF-alpha dans le corps sont associés à une sensibilité accrue aux allergies. Cette substance peut également être impliquée dans le développement de l'asthme. Les scientifiques associent désormais la genèse de nombreuses maladies auto-immunes à des niveaux anormaux de facteurs de croissance dans le corps.
TNF-alpha en tant que médicament
L'histoire du TNF-alpha en médecine a commencé à la fin du 19e siècle. William Coley, chirurgien basé à New York, a observé un rétrécissement de la tumeur maligne après une injection topique de bactéries streptocoques Streptococcus pyogenes. Dans la prochaine étape du travail, le chercheur a commencé à utiliser des micro-organismes tués par haute température. Des études ont montré que le rétrécissement de la tumeur n'était pas associé aux bactéries vivantes elles-mêmes, mais aux substances qui font partie de leurs parois cellulaires. La nécrose hémorragique du fibrosarcome s'est développée chez des animaux de laboratoire recevant des polysaccharides, qui font partie des parois cellulaires bactériennes.
En 1975, une cytokine a été isolée qui se forme dans la réponse immunitaire au polysaccharide bactérien découvert par William Coley. Il s'est avéré que c'est cette protéine immunitaire, et non des substances bactériennes, qui provoque la nécrose hémorragique des tumeurs. La substance a été nommée "facteur de nécrose tumorale alpha"ou TNF-alpha pour faire court.
Le facteur de nécrose tumorale alpha a été utilisé comme médicament anticancéreux. En raison de son fort effet toxique sur l'organisme, il ne peut pas être administré par voie systémique. Il n'est utilisé que par voie topique pour traiter les tumeurs. Des recherches sont toujours en cours pour modifier cette substance afin d'obtenir un médicament à toxicité réduite et à efficacité accrue.
Inhibiteurs du TNF-alpha en tant que médicaments
Les inhibiteurs du TNF sont des médicaments qui suppriment la réponse physiologique au facteur de nécrose tumorale (TNF) dans le cadre de la réponse inflammatoire.
Le facteur de nécrose tumorale est impliqué dans le développement de maladies auto-immunes et immunitaires. Ce groupe de troubles comprend des maladies telles que:
- polyarthrite rhumatoïde
- spondylarthrite ankylosante
- maladie inflammatoire de l'intestin
- psoriasis
- pyoderma
- asthme réfractaire
Par conséquent, des recherches sont toujours en cours sur de nouveaux inhibiteurs du TNF qui pourraient être utilisés dans le traitement de ces maladies.
En raison du rôle du TNF-alpha dans l'élimination des cellules cancéreuses, les inhibiteurs de cette protéine stimulent la formation de changements néoplasiques tels que les lymphomes. Les autres effets secondaires de ces médicaments comprennent:
- infections (en particulier réactivation de la tuberculose latente)
- insuffisance cardiaque
- induction d'autoanticorps
- réactions au site d'injection
L'inhibition de l'activité du TNF peut être obtenue avec des anticorps monoclonaux. Ce groupe de médicaments comprend:
- infliximab
- adalimumab
- certolizumab
- golimumab
Le blocage de l'activité du TNF peut également être induit en utilisant une protéine réceptrice recombinante qui bloque le récepteur du facteur de nécrose tumorale. Le médicament qui agit de cette manière est l'étanercept.
Inhibiteurs du TNF dans le traitement de la polyarthrite rhumatoïde
Il a été démontré que le facteur de nécrose tumorale joue un rôle clé dans le développement de la polyarthrite rhumatoïde. Il a été démontré que les taux de TNF augmentent à la fois dans le liquide synovial et dans la synovie des patients atteints de polyarthrite rhumatoïde. Cela conduit à une inflammation locale.
L'utilisation clinique des inhibiteurs du TNF dans la polyarthrite rhumatoïde a été prouvée par Marc Feldmann et Ravinder N. Mainia. Les médicaments anti-TNF aident à éliminer l'activité anormale des cellules B responsables du développement de la maladie.
Un traitement associant des inhibiteurs du TNF et du méthotrexate s'est également avéré plus efficace pour restaurer la qualité de vie des personnes souffrant de polyarthrite rhumatoïde par rapport à une monothérapie.
Inhibiteurs du TNF dans le traitement du cancer
En raison de la participation précédemment décrite du TNF dans la formation de métastases, les inhibiteurs de cette substance ont trouvé une application en tant que médicaments anticancéreux potentiels.
La thérapie anti-TNF n'a montré qu'une efficacité modérée dans le traitement du cancer.
L'infliximab, un inhibiteur du TNF-alpha, produit une stabilisation prolongée de la maladie chez certains patients.
Un autre médicament de ce groupe, l'étanercept, a été étudié dans le traitement de patientes atteintes d'un cancer du sein et d'un cancer de l'ovaire. Il a également montré une stabilisation de l'état de la maladie chez les patients.
En revanche, les études sur l'utilisation de ces médicaments dans le traitement de patients atteints d'un cancer du pancréas avancé n'ont pas montré une efficacité satisfaisante par rapport au placebo.
Inhibiteurs naturels du TNF
Des études récentes montrent que les substances actives contenues dans les plantes peuvent également avoir la capacité d'inhiber le TNF-alpha. Ces propriétés ont la curcumine trouvée dans le curcuma et les catéchines dérivées du thé vert.
Il existe également des études suggérant que les propriétés anti-inflammatoires du cannabis et de l'échinacée sont associées à l'inhibition du facteur de nécrose tumorale.
Sources:
- Le rôle du facteur de nécrose tumorale (TNF) et de ses récepteurs dans la parodontite d'après la littérature, Anna Maria Wasilewska, Sylwia Małgorzata Słotwińska Borgis - Nowa Stomatologia 1/2003, pp. 49-51
- Récepteurs de la mort - la cible moléculaire des médicaments anticancéreux, prof. dr hab. ZDZISŁAW CHILMONCZYK, GAZETA PHARMACEUTYCZNA 1/2009
- Wajant H, Pfizenmaier K, Scheurich P (2003). "Signalisation de facteur de nécrose tumorale". Différence de mort cellulaire. 10 (1): 45–65. accès en ligne
- Chen G, Goeddel DV (2002)."Signalisation TNF-R1: une belle voie". Science.296 (5573): 1634–5., Accès en ligne
- Gaur U, Aggarwal BB (2003). "Régulation de la prolifération, de la survie et de l'apoptose par les membres de la superfamille TNF". Biochem. Pharmacol. 66 (8): 1403–8. accès en ligne
- Raduner S, Majewska A, Chen JZ, Xie XQ, Hamon J, Faller B, Altmann KH, Gertsch J (mai 2006). "Les alkylamides de l'échinacée sont une nouvelle classe de cannabinomimétiques. Effets immunomodulateurs dépendants et indépendants des récepteurs cannabinoïdes de type 2". J. Biol. Chem. 281 (20): 14192-206. accès en ligne
- Korneev, KV; Atretkhany, KN; Drutskaya, MS; Grivennikov, SI; Kuprash, DV; Nedospasov, SA (janvier 2017). "TLR-signalisation et cytokines pro-inflammatoires en tant que conducteurs de la tumorigenèse". Cytokine. 89: 127-135. accès en ligne
- Feldmann M, Maini RN (octobre 2003). "Prix de recherche médicale clinique Lasker. TNF défini comme une cible thérapeutique pour la polyarthrite rhumatoïde et d'autres maladies auto-immunes". Nat. Med. 9 (10): 1245–50. accès en ligne

Lire plus d'articles de cet auteur